Fique por dentro das novidades
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!

Óxido de ferro II pode ser reduzido a ferro, tanto por carbono, como por monóxido de carbono, de acordo com o mostrado nas equações 1 e 2:
Os calores de entalpia de formação e de entropia-padrão das substâncias envolvidas em ambas as reações são apresentados na tabela:
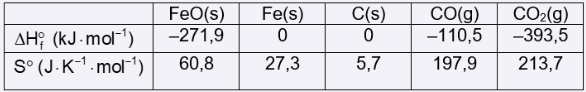
Considere um meio reacional fechado onde ocorrem as duas reações e que os valores acima permanecem constantes na faixa de 298 a 650 K.
A ÚNICA alternativa correta é:
A reação 1 é exotérmica e a reação 2 é endotérmica.
À temperatura aproximada de 627 K, a reação 2 atinge o equilíbrio dinâmico.
À temperatura de 450 K, a reação 1 é fonte de calor para sustentar a reação 2 na proporção molar aproximada de 15 para 1.
À temperatura de 450 K, ambas as reações são espontâneas.
A reação 1 apresenta diminuição de entropia.
Para a reação 1:
Para a reação 2:
Para a reação 1:
Para a reação 2:
Para o equilíbrio da reação 2:
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!